Malformations de l’utérus : résumé
|
Crédits images : Case courtesy of Dr Frank Gaillard, Radiopaedia.org. From the case rID: 11115
Malformations de l’utérus : résumé
|
Crédits images : Case courtesy of Dr Frank Gaillard, Radiopaedia.org. From the case rID: 11115
Préparation pour l’exploration de la statique pelvienne
|
Séquences IRM
|
Analyse dynamique de la statique pelvienne
|
Résultats
|
Adénomyose
|
|
Généralités
|
ÉCHOGRAPHIE
|
IRM
|
|
|
|
CRITÈRES SÉMIOLOGIQUES DE la grossesse extra utérine
|
|
|
|
images pièges
|
|
|
|
Compte rendu
|
|
|
|
Myomes utérins
|
|||
Généralités
|
Echographie
|
||
IRM
|
Ce que doit comporter le Compte rendu
|
||
DD
|
Indication de la myomectomie par cœlioscopie
|
||
PROTOCOLE D’EXPLORATION par hystérographie
|
|
|
|
CAUSES TUBAIRES D’INFERTILITÉ |
|
|
CAUSES UTÉRINES D’INFERTILITÉ |
|
|
Type 1 – Kyste liquidien pur |
|
Syndrome des ovaires polykystiques |
|
|
Type 2 – Kyste multiloculaire |
|
Type 3 – Kyste endométriosique (endométriome) |
Échographie
|
IRM
|
Type 4 – Kyste contenant des végétations |
|
Type 5 – le kyste à parois / cloisons épaisses ou nodule solide |
|
Type 6 – Tumeur ovarienne solide pure |
|
| Score O-RADS-IRM |
| Le score O-RADS-IRM classe en 5 catégories de risque de malignité les masses annexielles considérées complexes ou indéterminées en échographie. Le score O-RADS IRM 1 correspond à l’absence de lésion annexielle (disparition de la lésion en IRM ou présence d’une lésion non annexielle). Le score O-RADS IRM 2 correspond à des lésions bénignes avec un faible risque de malignité (VPP < 2%). Il s’agit soit de lésion liquidienne pure (cystadénome séreux bénin, kyste folliculaire), graisseuse majoritaire (tératome mature) ou endométriosique (endométriome) (Figure 1) ou bien de lésion avec une portion tissulaire en hyposignal T2 et hyposignal diffusion. Pour rappel, une portion tissulaire est définie en IRM comme des cloisons irrégulières, un nodule mural, des végétations ou une masse solide (>80% de portion tissulaire) se rehaussant après injection de gadolinium. Ces lésions O-RADS IRM 2 ne nécessitent pas de suivi particulier. Le score O-RADS IRM 3 correspond à des lésions probablement bénignes (VPP<5%). Il s’agit soit de lésions liquidiennes dont le contenu n’est pas strictement liquidien pur, graisseux majoritaire ou endométriosique, soit de lésions liquidiennes multiloculaires ou bien de lésions avec une portion tissulaire se rehaussant selon une courbe de type 1 (rehaussement initial moins important que le myomètre avec une augmentation progressive et faible sans plateau) (Figure 2). Les lésions O-RADS 3 nécessitent une surveillance rapprochée par échographie ou IRM afin de vérifier la stabilité de la taille sur 2 ans. Le score O-RADS IRM 4 correspond à des lésions indéterminées en IRM (VPP de 5 à 95 %). Il s’agit de masses avec portion tissulaire et une courbe de rehaussement de type 2 (rehaussement initial non pré décalé par rapport au myomètre avec une augmentation progressive et modérée avec plateau). Pour le score O-RADS IRM 4, il est primordial de donner des orientations anatomopathologiques car il peut s’agir de lésions bénignes, malignes ou borderline débouchant sur une prise en charge différente. Ces lésions O-RADS IRM 4 nécessitent une prise en charge chirurgicale dans un centre de référence. Le score O-RADS IRM 5 correspond à des lésions de risque de malignité très élevé (VPP >95%). Le score 5 est lié soit à la présence d’implants péritonéaux soit à la présence d’une portion tissulaire avec une courbe de type 3 (rehaussement initial pré décalé par rapport au myomètre avec augmentation importante et plateau) (Figure 3). Ces lésions nécessitent de réaliser un bilan d’extension par un TDM thoraco abdomino pelvienne et une prise en charge chirurgicale dans un centre de référence avec indication théorique de cyto-réduction d’emblée. |
Cancer du col utérin
|
|
|
|
Endométriose pelvienne
|
|
échographie
|
|
IRM
Lésions élémentaires
|
|
coelioscopie |
BHCG
|
|
|
|
Embryon
|
|
|
|
/!\ Ces valeurs sont une estimation /!\
(Cf. SAlomon LJ. Comment déterminer la date de début de grossesse ? Recommandations pour la pratique clinique J Gynecol Obstet Biol Reprod, 2011.40:726-33)
| LCC (mm) | Age gestationnel (Robinson) |
| 6 | 6 SA + 1 |
| 7 | 6 SA + 3 |
| 8 | 6 SA + 5 |
| 9 | 6 SA + 6 |
| 10 | 7 SA + 0 |
| 11 | 7 SA + 1 |
| 12 | 7 SA + 3 |
| 13 | 7 SA + 4 |
| 14 | 7 SA + 5 |
| 15 | 7 SA + 6 |
| 16 | 8 SA + 0 |
| 17 | 8 SA + 1 |
| 18 | 8 SA + 2 |
| 19 | 8 SA + 3 |
| 20 | 8 SA + 4 |
| 21 | 8 SA + 5 |
| 22 | 8 SA + 5 |
| 23 | 8 SA + 6 |
| 24 | 9 SA + 0 |
| 25 | 9 SA + 1 |
| 26 | 9 SA + 2 |
| 27 | 9 SA + 3 |
| 28 | 9 SA + 3 |
| 29 | 9 SA + 4 |
| 30 | 9 SA + 5 |
| 31 | 9 SA + 6 |
| 32 | 9 SA + 6 |
| 33 | 10 SA + 0 |
| 34 | 10 SA + 1 |
| 35 | 10 SA + 1 |
| 36 | 10 SA + 2 |
| 37 | 10 SA + 3 |
| 38 | 10 SA + 3 |
| 39 | 10 SA + 4 |
| 40 | 10 SA + 5 |
| 41 | 10 SA + 5 |
| 42 | 10 SA + 6 |
| 43 | 10 SA + 7 |
| 44 | 11 SA + 0 |
| 45 | 11 SA + 1 |
| 46 | 11 SA + 1 |
| 47 | 11 SA + 2 |
| 48 | 11 SA + 3 |
| 49 | 11 SA + 3 |
| 50 | 11 SA + 4 |
| 51 | 11 SA + 4 |
| 52 | 11 SA + 5 |
| 53 | 11 SA + 5 |
| 54 | 11 SA + 6 |
| 55 | 11 SA + 6 |
| 56 | 12 SA + 0 |
| 57 | 12 SA + 1 |
| 58 | 12 SA + 1 |
| 59 | 12 SA + 2 |
| 60 | 12 SA + 2 |
| 61 | 12 SA + 3 |
| 62 | 12 SA + 3 |
| 63 | 12 SA + 4 |
| 64 | 12 SA + 4 |
| 65 | 12 SA + 5 |
| 66 | 12 SA + 5 |
| 67 | 12 SA + 6 |
| 68 | 12 SA + 6 |
| 69 | 13 SA + 0 |
| 70 | 13 SA + 0 |
| 71 | 13 SA + 1 |
| 72 | 13 SA + 1 |
| 73 | 13 SA + 2 |
| 74 | 13 SA + 2 |
| 75 | 13 SA + 2 |
| 76 | 13 SA + 3 |
| 77 | 13 SA + 3 |
| 78 | 13 SA + 4 |
| 79 | 13 SA + 4 |
| 80 | 13 SA + 5 |
| 81 | 13 SA + 5 |
| 82 | 13 SA + 6 |
| 83 | 13 SA + 6 |
| 84 | 14 SA + 0 |
| 85 | 14 SA + 0 |
Clinique de l’hyperplasie de l’endomètre
|
Classification de l’hyperplasie de l’endomètre
|
Echographie
|
Contre indications à l’IRM
|
|
|
Protocole
|
|
|
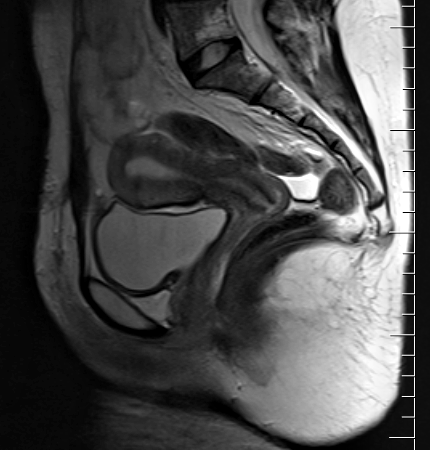 |
Séquences
|
|
|
|
Bilan d’extension du cancer de l’ovaire
|
|
Technique
|
|
Dissémination
|
|
Traitements
|
|
Pathologies tubaires
|
|
Hydro-salpinx
|
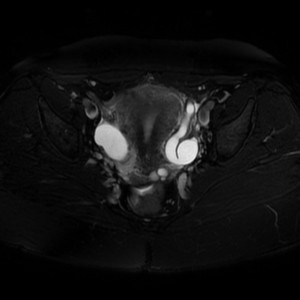 |
Pyosalpinx
|
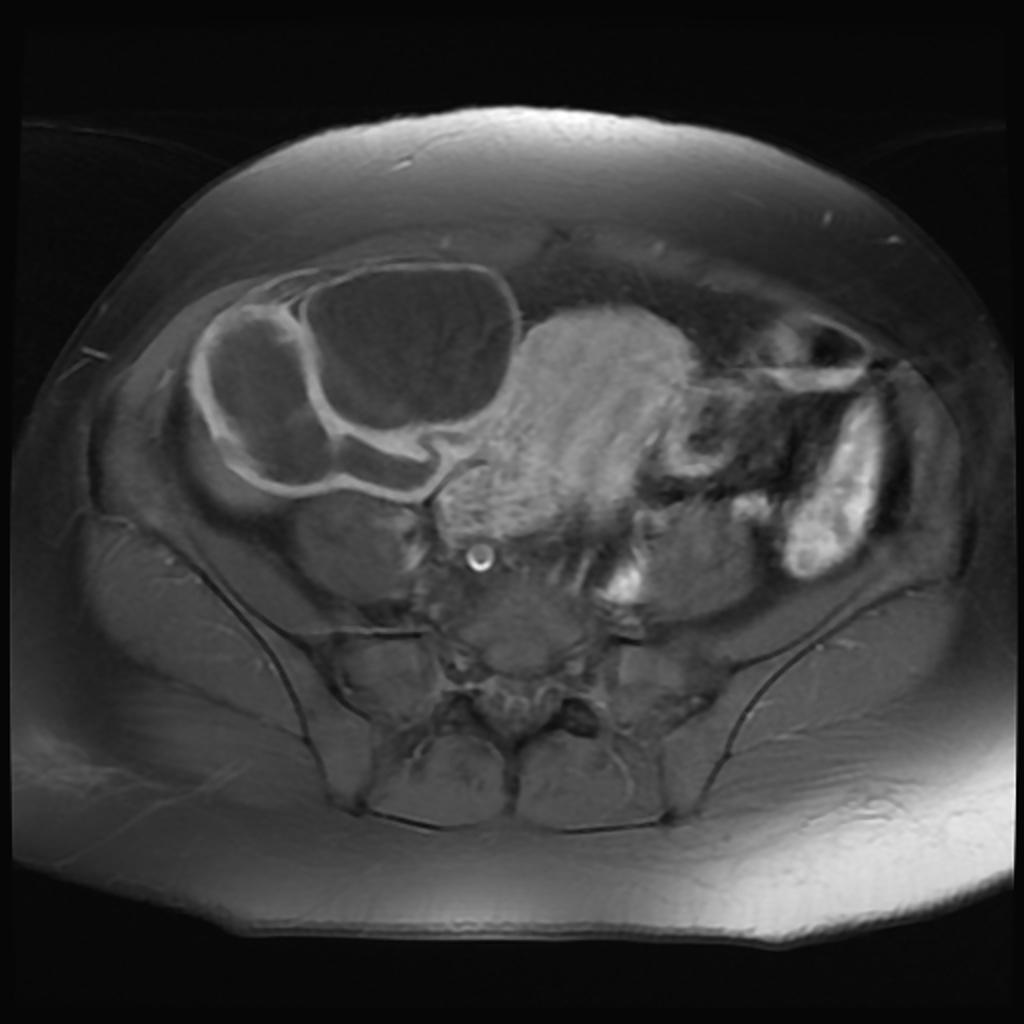 |
Kyste para-tubaire |
|
Cancer de la trompe |
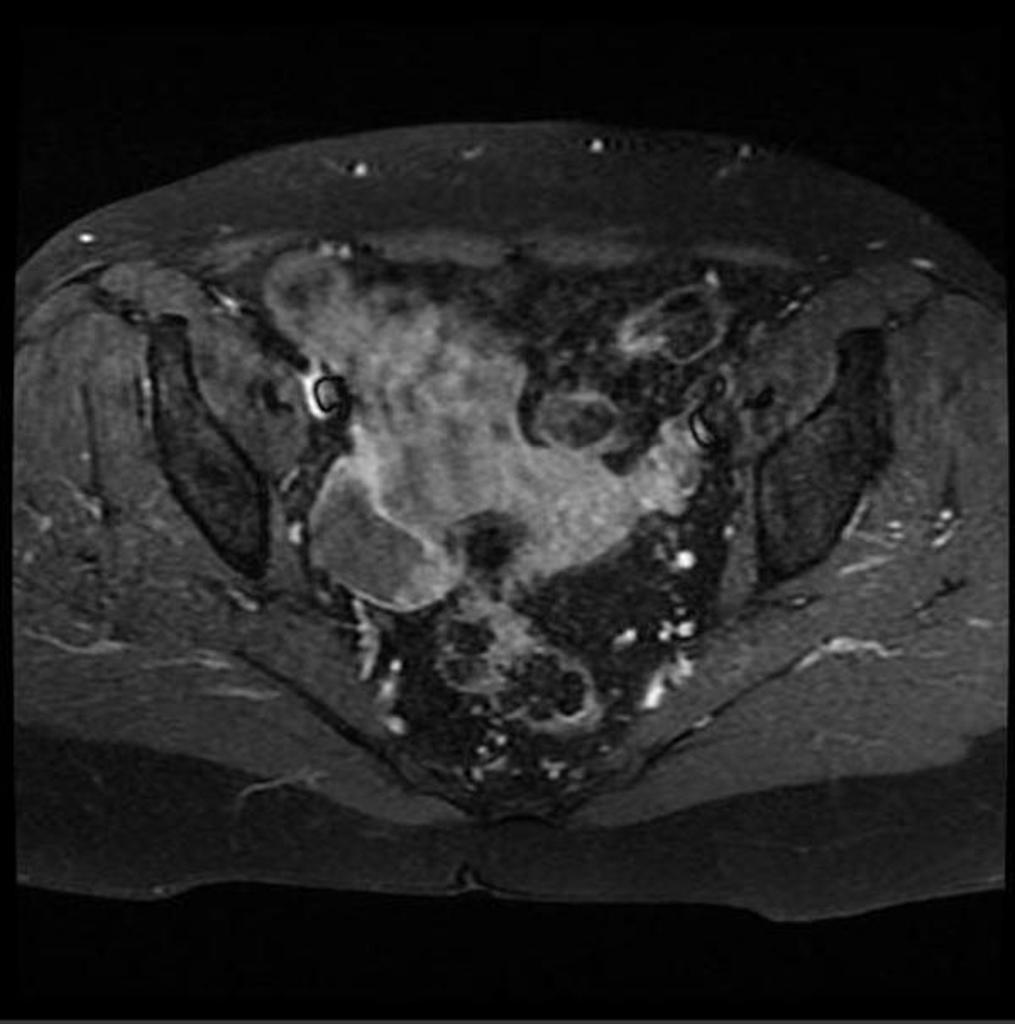 Case courtesy of Radiopaedia.org. From the case rID: 11817 Case courtesy of Radiopaedia.org. From the case rID: 11817 |
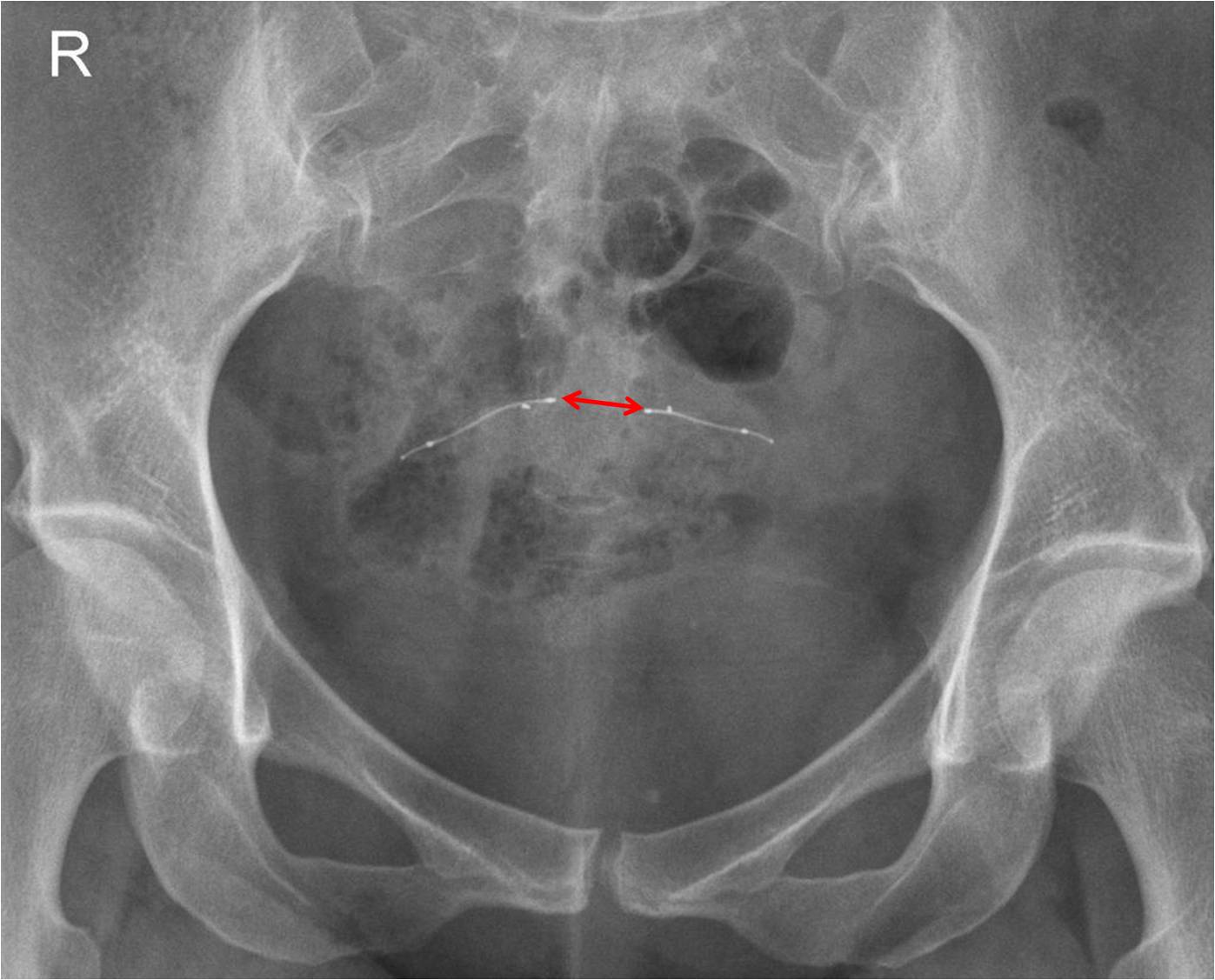
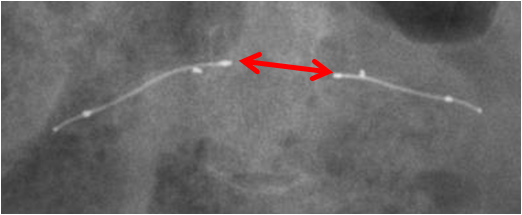
Contrôle du bon positionnement des dispositifs Essure ®
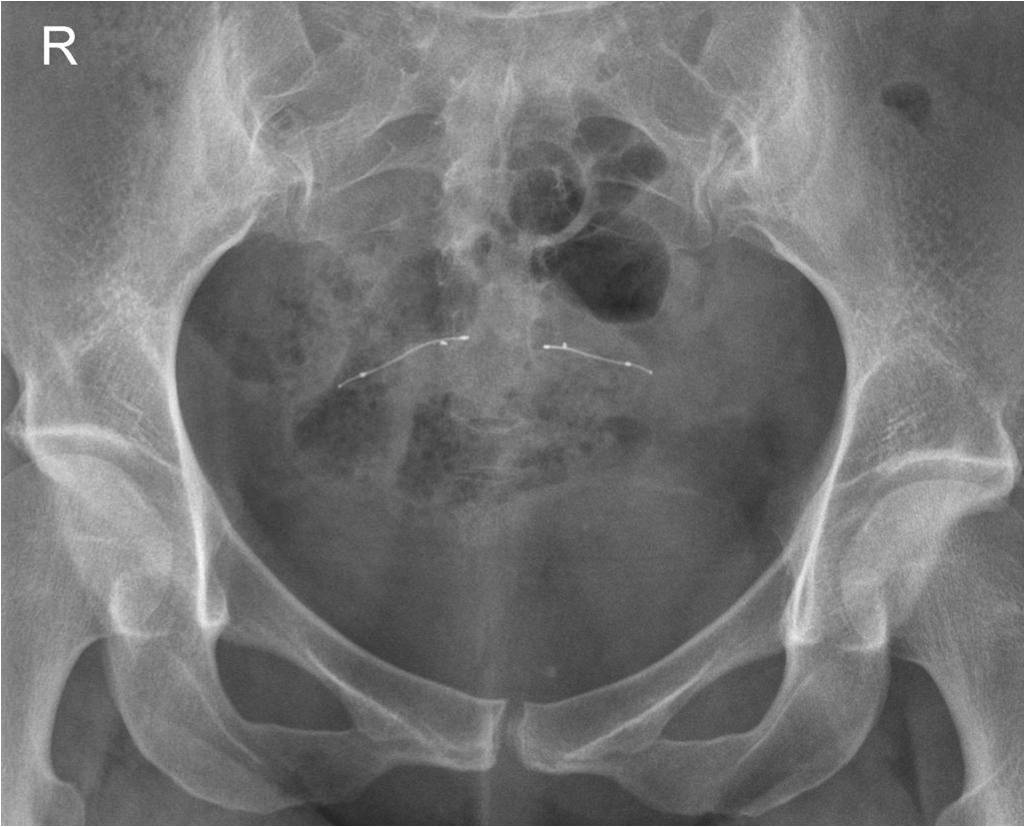 Réaliser un ASP de face stricte et éventuelle rotation pour être dans le plan de l’utérus.
Réaliser un ASP de face stricte et éventuelle rotation pour être dans le plan de l’utérus.
| FIGO (2009) | TNM (2009) | Description |
|---|---|---|
| Stade I | T1 | Tumeur limitée aux ovaires |
| IA | T1a | Un ovaire, capsule intacte, cytologie péritonéale négative |
| IB | T1b | Deux ovaires, capsules intactes, cytologie péritonéale négative |
| IC | T1c | Un ou deux ovaires ou rupture capsulaire ou cytologie péritonéale positive |
| Stade II | T2 | Tumeur limitée au pelvis |
| IIA | T2a | Extension à l’utérus ou aux trompes, cytologie péritonéale négative |
| IIB | T2b | Extension aux autres organes du pelvis (vessie, colon, rectum), cytologie péritonéale négative |
| IIC | T2c | IIA ou IIB + cytologie péritonéale positive |
| Stade III | T3 et/ou N1 | Tumeur limitée à l’abdomen |
| IIIA | T3a | Extension péritonéale microscopique |
| IIIB | T3b | Extension péritonéale ≤ 2cm |
| IIIC | T3c | Extension péritonéal > 2cm |
| N1 | Atteinte des ganglions lymphatiques régionaux | |
| Stade IV | T4 et/ou M1 | Métastases à distance |
Source : HAS 2010
| Stade I – Cancer strictement limité au col | ||
| Stade IA – Cancer invasif identifié seulement au microscope et envahissement du stroma : profondeur maximum de 5 mm | IA1 | profondeur ≤ 3 mm, largeur ≤ 7 mm |
| IA2 | 3 mm < profondeur ≤ 5 mm et largeur ≤ 7 mm | |
| Stade IB – Cancer clinique limité au col visible en macroscopie ou cancer microscopique de dimension supérieure au IA | IB1 | T <2 cm |
| IB2 | 2 ≤ T <4 cm | |
| IB3 | T ≥ 4 cm | |
| Stade II – Cancer étendu au-delà du col mais n’atteignant pas la paroi pelvienne ni le tiers inférieur du vagin | ||
| Stade IIA – jusqu’aux deux tiers supérieurs du vagin | IIA1 | Taille T ≤ 4 cm |
| IIA2 | Taille T >4 cm | |
| Stade IIB | paramètres (proximaux) | |
| Stade III – Cancer étendu jusqu’à la paroi pelvienne et/ou au tiers inférieur du vagin (y compris hydronéphrose) | Stade IIIA | Atteinte vaginale jusqu’au tiers inférieur |
| Stade IIB | Fixation à la paroi pelvienne (ou hydronéphrose ou rein muet) | |
| Stade IIIC | IIIC1 | Atteinte ganglionnaire pelvienne * |
| IIIC2 | Atteinte ganglionnaire lombo-aortique * | |
| Stade IV – Cancer étendu au-delà du petit bassin ou à la muqueuse vésicale et/ou rectale | Stade IVA | Organe adjacent (vessie, rectum) |
| Stade IVB | A distance |
| FIGO (2009) | TNM (2009) | Description |
|---|---|---|
| Stade I | T1 | Tumeur limitée au corps utérin |
| IA | T1a | Tumeur limitée à l’endomètre ou ne dépassant pas la moitié du myomètre |
| IB | T1b | Tumeur envahissant la moitié du myomètre ou plus de la moitié du myomètre |
| Stade II | T2 | Tumeur envahissant le stroma cervical mais ne s’étendant pas au-delà de l’utérus |
| Stade III | T3 et/ou N1 | Extensions locales et/ou régionales comme suit : |
| IIIA | T3a | Séreuse et/ou annexes |
| IIIB | T3b | Envahissement vaginal et/ou paramétrial |
| IIIC | N1 | Atteinte des ganglions lymphatiques régionaux |
| IIIC1 | Ganglions pelviens | |
| IIIC2 | Ganglions lomboaortiques ± ganglions pelviens | |
| Stade IV | T4 et/ou M1 | Extension à la muqueuse vésicale et/ou intestinale et/ou métastases à distance |
| IVA | T4 | Extension à la muqueuse vésicale et/ou intestinale |
| IVB | M1 | Métastases à distance incluant les métastases intra-abdominales et/ou ganglions inguinaux |
Source : HAS 2010
| FIGO 2023 | Description |
|---|---|
| Stade I | Limité au corps utérin et à l’ovaire |
| IA | Disease limited to the endometrium OR non-aggressive histological type, i.e. low-grade endometroid, with invasion of less than half of myometrium with no or focal lymphovascular space involvement (LVSI) OR good prognosis disease |
| IA1 Non-aggressive histological type limited to an endometrial polyp OR confined to the endometrium | |
| IA2 Non-aggressive histological types involving less than half of the myometrium with no or focal LVSI | |
| IA3 Low-grade endometrioid carcinomas limited to the uterus and ovary | |
| IB | Non-aggressive histological types with invasion of half or more of the myometrium, and with no or focal LVSI |
| IC | Aggressive histological types limited to a polyp or confined to the endometrium |
| Stade II | Invasion of cervical stroma without extrauterine extension OR with substantial LVSI OR aggressive histological types with myometrial invasion |
| IIA | Invasion of the cervical stroma of non-aggressive histological types |
| IIB | Substantial LVSI of non-aggressive histological types |
| IIC | Aggressive histological types with any myometrial involvement |
| Stade III | Local and/or regional spread of the tumor of any histological subtype |
| IIIA | Invasion of uterine serosa, adnexa, or both by direct extension or metastasis |
| IIIA1 Spread to ovary or fallopian tube (except when meeting stage IA3 criteria) IIIA2 Involvement of uterine subserosa or spread through the uterine serosa | |
| IIIB | Metastasis or direct spread to the vagina and/or to the parametria or pelvic peritoneum |
| IIIB1 Metastasis or direct spread to the vagina and/or the parametriaIIIB2 Metastasis to the pelvic peritoneum | |
| IIIC | Metastasis to the pelvic or para-aortic lymph nodes or both |
| IIIC1 Metastasis to the pelvic lymph nodesIIIC1i MicrometastasisIIIC1ii MacrometastasisIIIC2 Metastasis to para-aortic lymph nodes up to the renal vessels, with or without metastasis to the pelvic lymph nodesIIIC2i MicrometastasisIIIC2ii Macrometastasis | |
| Stade IV | Spread to the bladder mucosa and/or intestinal mucosa and/or distance metastasis |
| IVA | Invasion of the bladder mucosa and/or the intestinal/bowel mucosa |
| IVB | Abdominal peritoneal metastasis beyond the pelvis |
| IVC | Distant metastasis, including metastasis to any extra- or intra-abdominal lymph nodes above the renal vessels, lungs, liver, brain, or bone |
Bilan d’extension du cancer du corps utérin
|
|
Technique
Traitement
|
|
FIGO 2009
|
Utérus
|
|
|
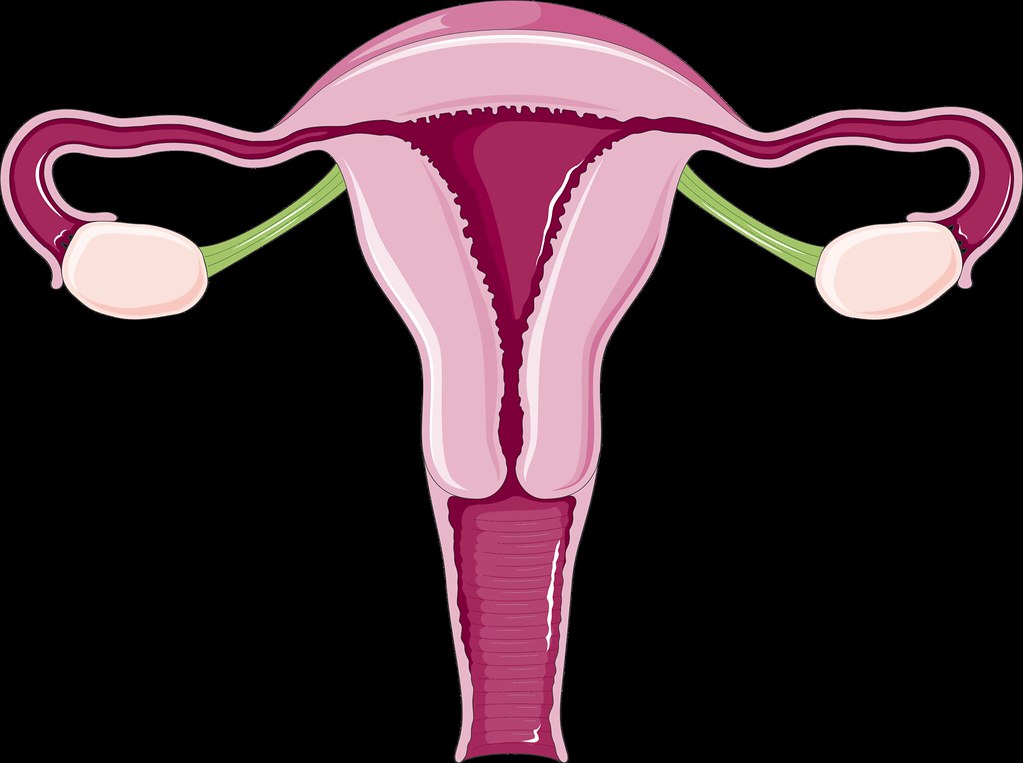 |
Myomètre externe [IsoT2]
|
|
|
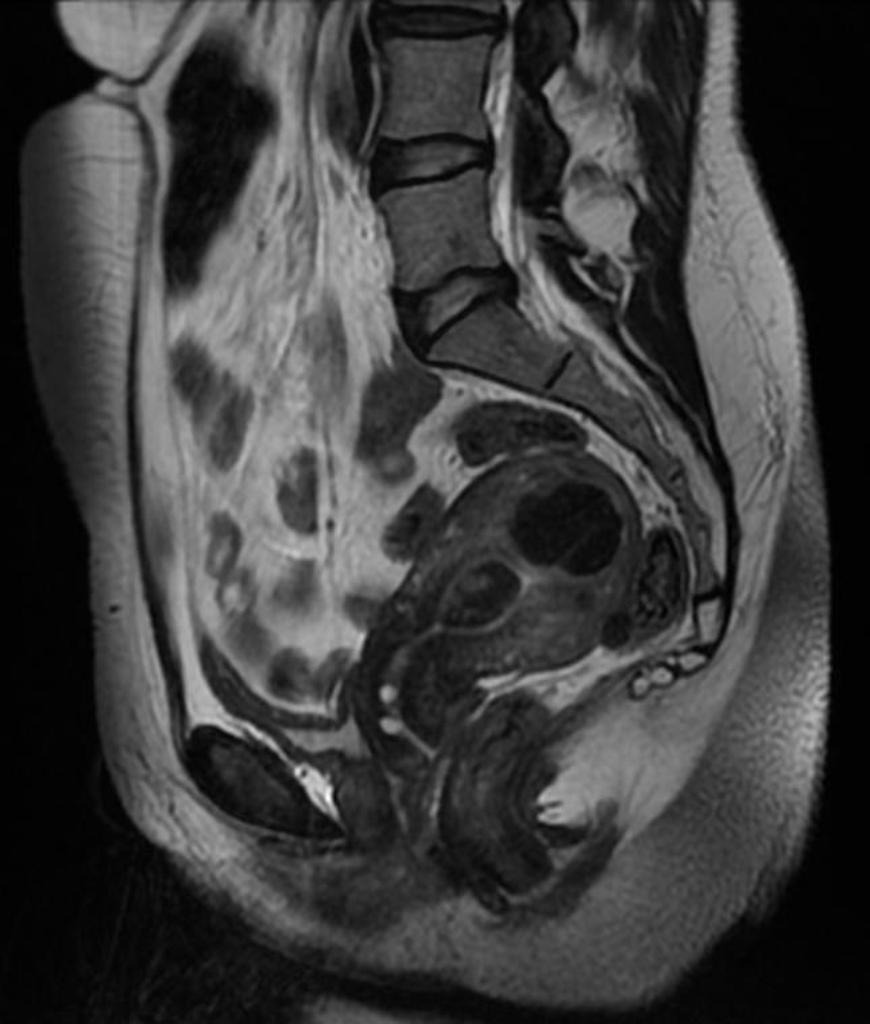 Case courtesy of Radiopaedia.org. From the case rID: 12063 |
TITRE_XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX
|
|
|
IMAGES_ICI |
Échographie pelvienne
|
|
| Col |
|
| Utérus |
|
| Endomètre |
|
| Ovaires |
|
| Tumeur ovarienne : critères simples pour tumeurs bénignes | Tumeur ovarienne : critères simples pour malignité́ |
|
|
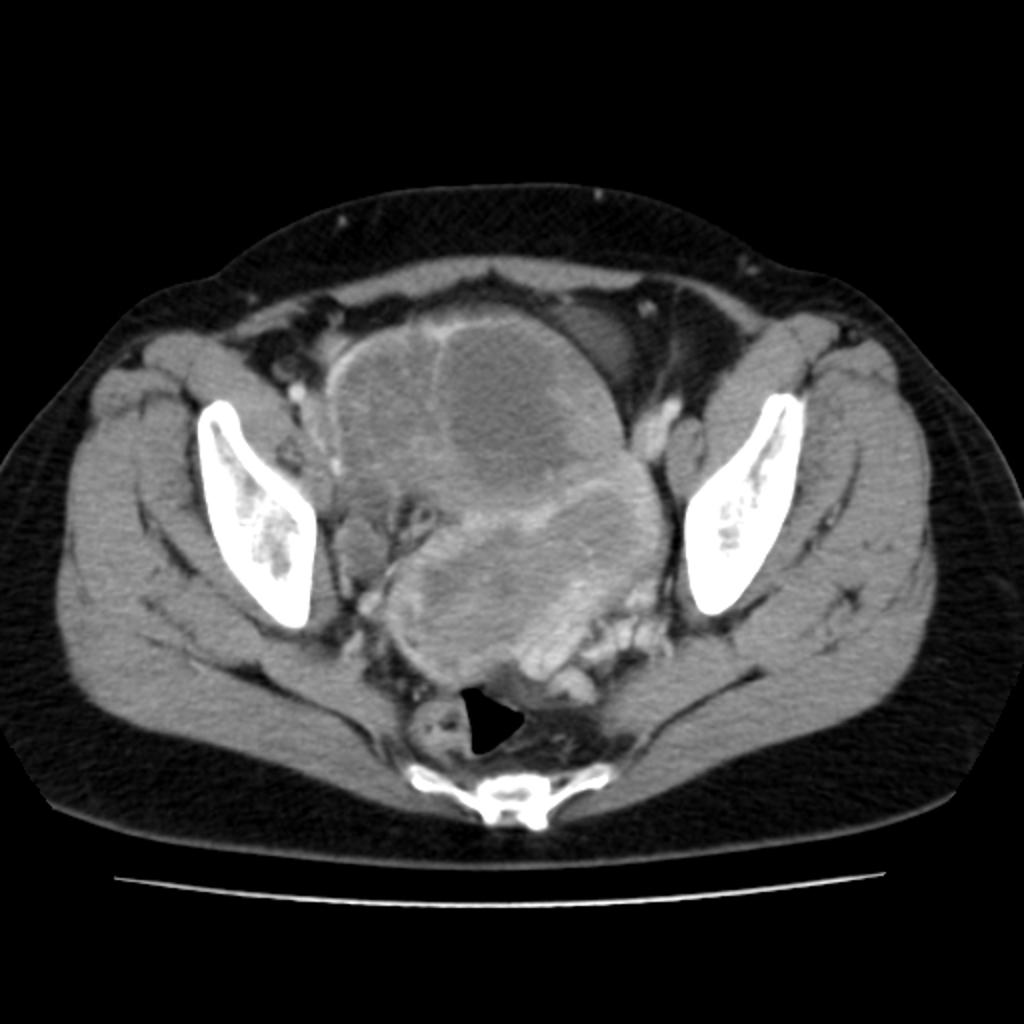
Cancer de l’endomètre
|
|
|
 |