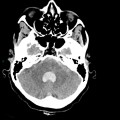
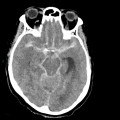
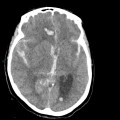
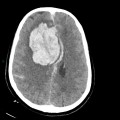
Classification de Fischer modifiée de l’hémorragie méningée
- Grade 0 : Absence de sang dans les citernes ou ventricules
- Grade 1 : HSA minime, pas d’hémorragie ventriculaire dans les 2 ventricules latéraux
- Grade 2 : HSA minime, hémorragie ventriculaire dans les 2 ventricules latéraux
- Grade 3 : HSA importante, pas d’hémorragie ventriculaire dans les 2 ventricules latéraux
- Grade 4 : HSA importante, hémorragie ventriculaire dans les 2 ventricules latéraux
|
Etiologies des HSA non traumatiques
- Rupture d’anévrisme 85%
Hémorragie méningée
- Hémorragie périmésencéphalique 10%
- autres causes rares 05%
- Dissections intracrâniennes
- MAVs
- Fistules durales
- MAVs médullaires
- Anévrismes septiques
- Artérites cérébrales
- Thromboses veineuses cérébrales (HSA de la convexité)
- Clinique douteuse + TDM normal = angioTDM
- Clinique douteuse + imagerie normale = PL
- Si vasospasme clinique : faire imagerie de diffusion et imagerie de perfusion
- Dépistage familial par angio MR proposé lorsque 2 membres de la même lignée ont présenté une rupture
|
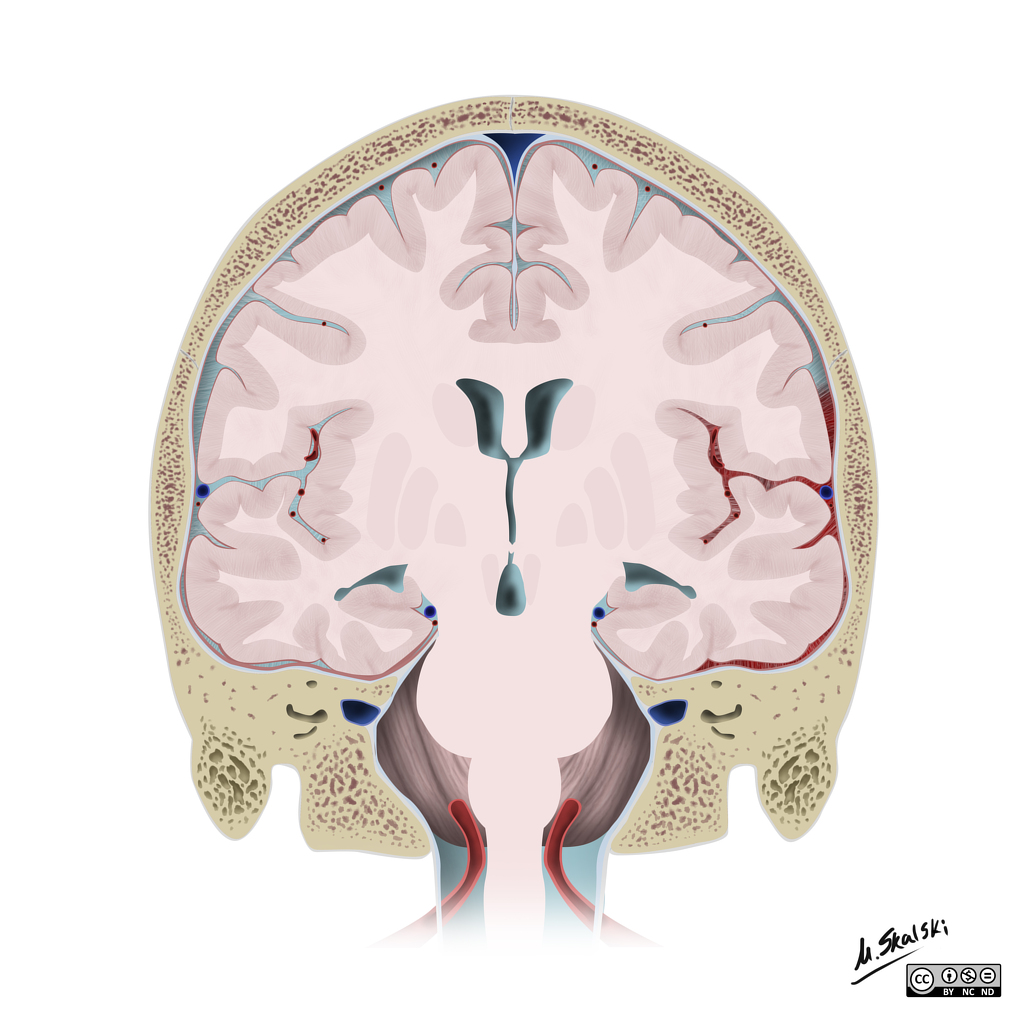 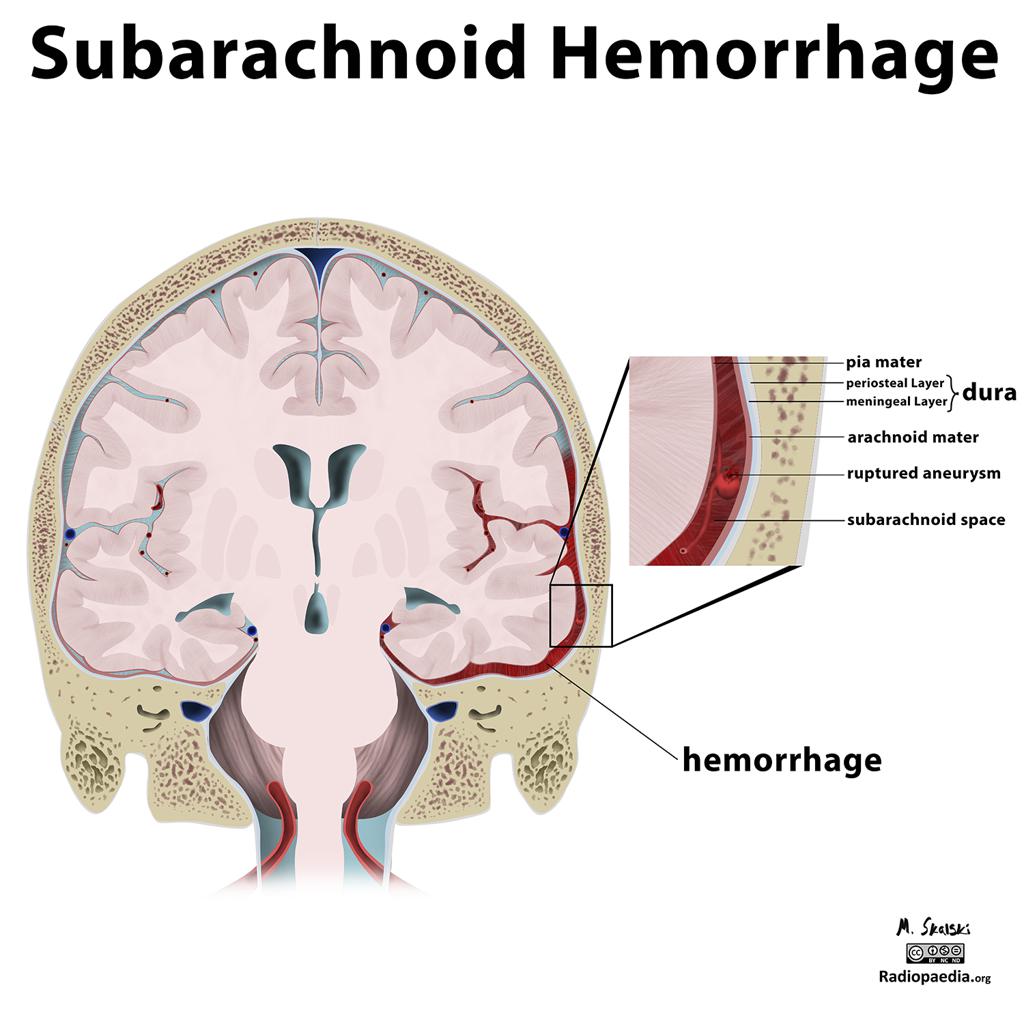
|
Article : hémorragie sous-arachnoidienne en 10 questions